ENLACES QUÍMICOS
Enlace químico: Es la fuerza que mantiene unidos a los átomos para formar moléculas elementales o compuestos. Son fuerzas de carácter eléctrico o electrostático (porque intervienen los electrones), para adquirir una fuerza estable y así poder permanecer o existir.
Tipos de enlace
| Enlace metálico | Los conductores por excelencia son los metales. Estos forman redes de iones en los que cada átomo cede sus electrones de valencia para formar una nube de electrones libres. La nube negativa hace de aglutinante de los iones positivos, apantallando la repulsión y manteniéndolos unidos. |
| Enlace iónico o electrovalente | Es aquel que se presenta cuando existe la transferencia completa de electrones de un átomo a otro, generalmente se da entre un metal (catión porque cede los electrones) y un no metal (anión porque gana los electrones) |
| Enlace covalente | Es aquel en el cual el par de electrones será compartido. Se presenta entre dos no metales. |
| Enlace covalente polar | Se presenta cuando los átomos son de diferente especie (diferente electronegatividad), los electrones se comparten de forma no equitativa entre los átomos y pasan más tiempo cerca de un átomo que del otro |
| Enlace covalente no polar | se forman entre dos átomos del mismo elemento o entre átomos de diferentes elementos que comparten electrones de manera más o menos equitativa. Tienen electronegatividad similar |
REGLA DEL OCTETO DE LEWIS
Los átomos de los elementos forman enlaces, tratan de tener ocho electrones externos. Se obtiene de tres maneras:
• Perdiendo hasta tres electrones como los metales formando un catión con la misma configuración electrónica del gas noble previo.
• Ganando hasta 3 electrones, como los no metales para formar un anión con la configuración electrónica del próximo gas noble.
• Los átomos (por lo general dos no metales) pueden compartir electrones con otros átomos para alcanzar el número de electrones del siguiente gas noble.
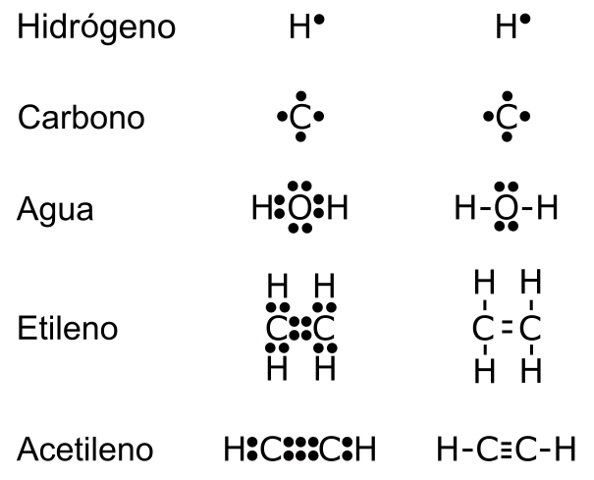
Observe que los electrónes son representados por puntos, y cuando hay dos que pueden formar un enlace, se pueden sustituir por una línea.
Recuerda que los electrones que pueden formar enlaces (se encuentran en el último nivel de energía) son conocidos como electrones de valencia.
Limitaciones de la regla del octeto:
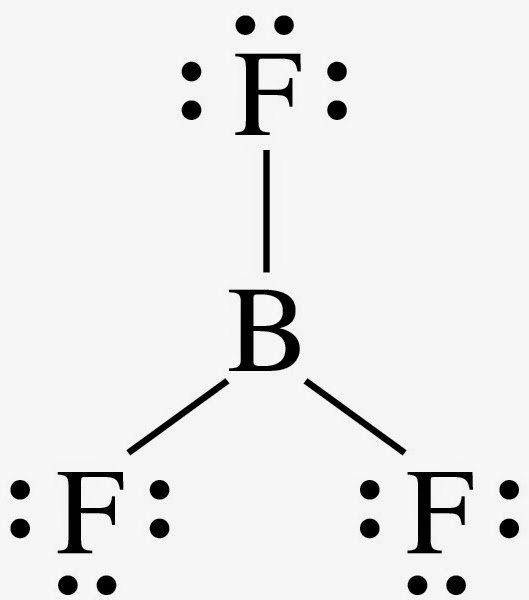
No explica la estructura de algunos compuestos como el BF3. En el que el átomo central no satisface la regla del octeto.