ELECTRONES,PROTONES Y NEUTRONES
| Partícula | Electrón | Protón | Neutron |
| Descubierta por | Thomson | Ernest Rutherford | James Chadwick |
| Año | 1897 | 1911 | 1932 |
| Carga eléctrica | Negativa | Positiva | Neutra |
| Ubicación en el átomo | Fuera del núcleo | Núcleo | Núcleo |
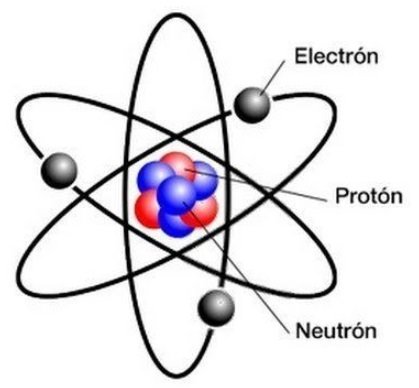
El numero atómico de un elemento indica la cantidad de protones que tiene en su núcleo.
Un elemento eléctricamente neutro tiene el mismo número de electrones que de protones.
La masa atómica de un elemento es igual a la suma de los protones más los neutrones. La masa de los electrones se considera despreciable.
Isótopos: Son átomos del mismo elemento que tienen el mismo número atómico pero diferente masa atómica (diferente cantidad de neutrones).

En algunos ejercicios pueden presentar el elemento con su respectiva infomación de la siguiente manera:
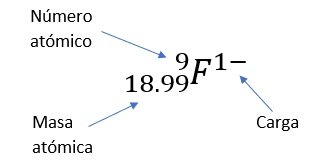
Si la carga es negativa se suman electrones (ganancia) y si es positiva se restan (pérdida)
| Ejemplos | |
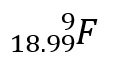
|
Elemento: Flúor Numero de masa: 19 Número atómico: 9 Protones: 9 Electrones: 9 Neutrones: 10 |
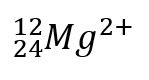
|
Elemento: Magnesio Numero de masa: 24 Número atómico: 12 Protones: 12 Electrones: 10 Neutrones: 12 |